O calor latente é a quantidade de energia térmica absorvida ou cedida por um corpo ou sistema termodinâmico. Isso em uma mudança do seu estado físico, com uma temperatura constante.
Sendo assim, o calor latente, também conhecido como calor de transformação, é uma grandeza física, já que aponta a quantidade de calor cedida ou recebida por um corpo durante a modificação do estado físico.
É importante notar que essa transformação de estado físico ocorre com a temperatura constante.
Por exemplo, um cubo de gelo que está derretendo, passa do estado sólido para líquido. Durante esse processo, a temperatura da água continua a mesma nos dois estados.
O cálculo do calor latente é feito por meio da fórmula: Q = mL. Onde o Q é a quantidade de calor transferido, o m é a massa do corpo e por fim, o L é o calor latente.
Em relação ao resultado do cálculo, o calor latente pode ter valores negativos ou positivos. Em resumo, se a substância estiver cedendo calor, o seu valor será negativo. Isso ocorre na solidificação e liquefação.
Em contrapartida, se a substância estiver recebendo calor, o valor será positivo. Desse modo, isso ocorre na fusão e na vaporização.
Tipos de calor latente
O calor pode ser latente, sensível ou específico. Em resumo, o calor latente ocorre quando há transferências de calor, sem que haja mudanças de temperatura. Sendo que ele se altera para as diferentes mudanças de estado físico.
Por outro lado, o calor sensível é transferido entre os corpos quando ocorrem mudanças de temperatura.
Por fim, o calor específico é a quantidade de calor necessária para aumentar a temperatura de 1 °C de 1g do elemento. Enfim, confira abaixo mais sobre esses tipos de calor:
1- Calor latente de vaporização
É o calor transferido em transformações sólido-líquido ou líquido-sólido. Isso em temperatura constante. Portanto, no calor latente de vaporização a substância passa por uma mudança de estado físico.
Sendo assim, se a mudança ocorrer da fase líquida para a fase gasosa, o calor latente é chamado calor de vaporização (Lv).
Por exemplo, o calor latente de vaporização da água é de 540 cal/g. Desse modo, são necessárias 540 cal para evaporar 1 g de água a 100 °C.
Portanto, a quantidade de calor necessária (Q) é proporcional à massa da substância (m):
Q = m . Lv
Sendo que o Lv é um valor constante que varia de acordo com a substância.
2- Calor sensível
O calor sensível causa mudanças de temperatura. Ou seja, trata-se de uma grandeza diferente do calor latente, já que a temperatura muda sem alterar o estado da substância.
Por exemplo, se aquecermos uma barra de metal, a temperatura irá aumentar. No entanto, o estado sólido da barra de metal não irá mudar. Enfim, a fórmula para calcular o calor sensível é:
Q = m . c . Δθ
Dessa forma, temos que:
Q é a quantidade de calor sensível (cal ou J)
m é massa do corpo (g ou Kg)
c é o calor específico da substância (cal/g°C ou J/Kg.°C)
Δθ é a variação de temperatura (°C ou K)
3- Calor específico
Por fim, temos o calor específico. Em síntese, esse tipo de calor é a quantidade de calor necessária para aumentar a temperatura de 1 °C de 1g do elemento.
Vale destacar que cada tipo de substância tem um calor específico, ou seja, trata-se de uma propriedade do material. O cálculo é feito com a fórmula:
c = Q / m . Δθ
ou
c = C / m
Sendo assim, na fórmula temos que:
c é o calor específico (cal/g°C ou J/Kg.K)
Q é a quantidade de calor (cal ou J)
m é a massa (g ou Kg)
Δθ é a variação de temperatura (°C ou K)
C é a capacidade térmica (cal/°C ou J/K)
Exemplos de calor latente
Para você entender melhor como é o calor latente no nosso dia a dia, vamos usar alguns exemplos:
1- Água na superfície quente
Se você jogar um pouco de água em uma superfície bem quente, a água irá evaporar de forma instantânea. Sendo assim, esse processo é chamado de calefação e envolve a absorção de calor latente.
2- Água para esquentar
Se você colocar água para esquentar, ela irá iniciar o processo de evaporação ao atingir a temperatura de 100 ºC. O que talvez você não saiba é que, enquanto a água vai evaporando, a sua temperatura não muda.
Fórmula
Em síntese, o cálculo é feito por meio da razão da quantidade de calor transferida na transformação isotérmica. Sendo assim, temos que:
Q = mL
L = Q / m
Q – quantidade de calor transferido
m – massa do corpo
L – calor latente
Mudanças de fases
Em substâncias puras, as mudanças de fases ocorrem em temperatura constante. Em resumo, isso acontece mediante a absorção ou liberação de calor latente.
Dessa forma, todas as substâncias puras apresentam uma curva de aquecimento que se parece com a da figura abaixo:
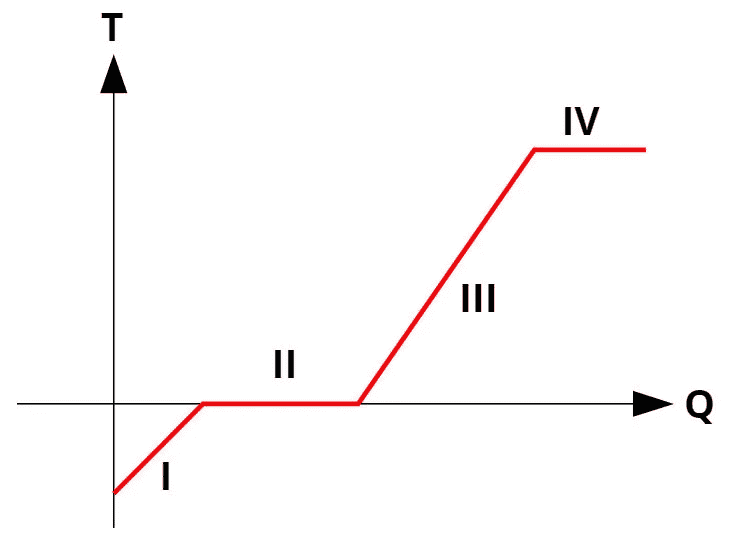
Dessa maneira, as curvas de aquecimento relacionam a temperatura (eixo y) com a quantidade de calor cedida ou recebida (eixo x).
Sendo assim, as mudanças de fase (processos II e IV), a temperatura permanece constante, mesmo que ocorram trocas de calor.
Dúvidas comuns
Algumas dúvidas comuns são:
1- O que é calor para a ciência?
Em síntese, o calor é a energia transferida de uma fonte quente para uma fonte fria.
2- Qual é a definição de calor latente?
O calor latente é a quantidade de energia térmica absorvida ou cedida por um corpo ou sistema termodinâmico. Isso em uma mudança do seu estado físico, com uma temperatura constante.
3- Qual o valor do calor latente de fusão?
Isso varia de acordo com a substância.
4- Quais são os tipos de calor latente?
O calor pode ser latente, sensível ou específico.
5- Como calcular Q ml?
Para usar a fórmula Q = mL e descobrir o calor latente (L) Você precisa dos valores de Q (quantidade de calor transferido) e m (massa do corpo).
6- Quais as características do calor latente?
Em resumo, o calor latente é caracterizado pela quantidade de energia ganha ou perdida por uma substância, em uma mudança de estado físico em temperatura constante.
7- Qual é o calor latente de fusão da água?
O calor latente de fusão da água corresponde a 80 cal/g.
8- Por que a água demora mais a esquentar?
A água demora mais a esquentar do que algumas outras substâncias, pois o específico da água é diferente de outras substâncias.
9- Em que situação o corpo pode perder calor latente?
Com o intuito de atingir equilíbrio térmico, o corpo humano sempre cede calor a um corpo mais “frio” que esteja em contato com ele.
Sendo assim, o calor passa de um corpo para o outro por causa da diferença de temperatura que existe entre eles.
10- Qual é a diferença entre o calor latente e calor específico?
Primeiramente, o calor latente é a quantidade de energia térmica absorvida ou cedida por um corpo ou sistema termodinâmico. Isso em uma mudança do seu estado físico, com uma temperatura constante.
Em contrapartida, o calor específico é a quantidade de calor necessária para aumentar a temperatura de 1 °C de 1g do elemento.
Fonte: Brasil Escola, Só Física, Wikipédia, Toda Matéria, Mundo Educação, Alunos Online, Info Escola, Vestibular, Colégio Web.
Bibliografia:
- HELERBROCK, Rafael. “Calor latente”; Brasil Escola. Acesso em 17 de julho de 2019.
- HALLIDAY, David (2011). Fundamentos de Física,8ª ed, vol 2. [S.l.]: LTC.
- EVANGELISTA, Carla Reis.Calor latente [20–] Infoescola Acesso em: 17 jul. 2019.



