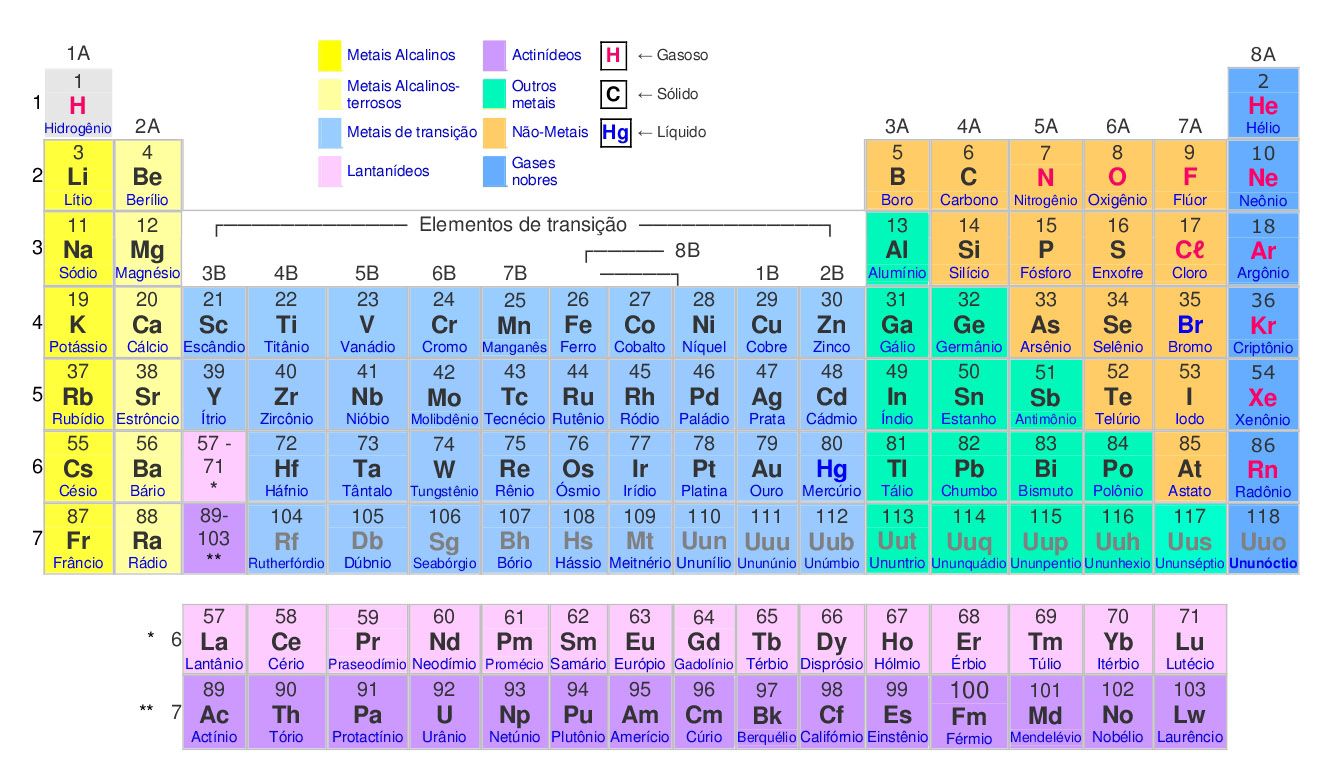
Elementos de transição, também conhecidos como Metais de transição, são elementos que possuem características intermediárias entre os metálicos – metais Alcalinos e Alcalino-terrosos -, à esquerda na Tabela Periódica, e os não metálicos.
Contudo, a localização foi proposta por Mendeleev e, na configuração atual da tabela, são as famílias de 3 a 12. Já as famílias restantes, compõem os chamados elementos representativos. Entretanto, os dois tipos apresentam diferenças marcantes.
Os elementos representativos são caracterizados por apresentarem elétrons mais energéticos nos subníveis s ou p. Por outro lado, na Tabela Periódica, os elementos de transição se caracterizam por apresentarem elétrons nos subníveis d ou f incompletos.
Tipos de elementos de transição
Estes elementos são conhecidos por apresentarem dois tipos diferentes: elementos de transição externa e elementos de transição interna.
Elementos de transição externa
Este tipo de elemento está localizado no centro da Tabela e seus elétrons mais energéticos estão no subnível d incompleto. Nesse sentido, apresentam orbitais de valência 3d, 4d e 5d (os mais energéticos).
Todavia, se apresentam em três níveis:
- Titânio, vanádio, cromo, manganês, ferro, cobalto, níquel e cobre.
- Zircônio, nióbio, molibdênio, tecnécio, rutênio, ródio, paládio e prata.
- Háfnio, tantálio, tungstênio, rênio, ósmio, irídio, platina e ouro.
Elementos de transição interna
São os elementos da série dos lantanídeos, que constituem os elementos com número atômico 57 até o número 71 e, da série dos actinídeos, com números de 83 a 103.

Todavia, são assim chamados por se localizarem na parte de baixo da Tabela Periódica. Seus elétrons mais energéticos estão localizados no subnível f incompleto. Nesse sentido, lantanídeos e actinídeos apresentam orbitais de valência 4f e 5f.
Você sabia?
1 – Estes elementos, tanto os internos quanto os externos, são classificados como metais e, por isso, possuem alta condutividade térmica e elétrica.
2 – Nesse sentido, os metais de transição são compostos por um grupo de elementos densos, que apresentam alto ponto de fusão e ebulição.

3 – Todavia, esses elementos são também menos reativos do que os elementos da família 1ª e 2ª da Tabela Periódica.
4 – O tungstênio é o elemento de transição com maior ponto de fusão, cerca de 3422° C. Já o mercúrio (Hg), além de se apresentar em estado líquido (CNTP), possui ponto de fusão em -38,83°C.
Então, o que achou da matéria? Se gostou, leia também: O que é energia? Definição, principais formas de energia e características.
Fontes: Brasil Escola, Manual da Química, Mundo Educação
Imagens: Espaço Ciência Viva, Físico-química 8º e 9ºano, Núcleo Visual, Mundo Educação, Coppermetal



